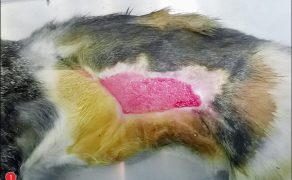
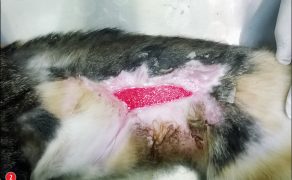
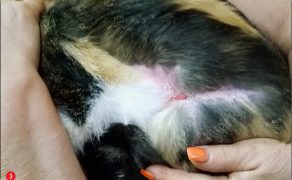
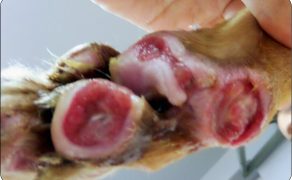
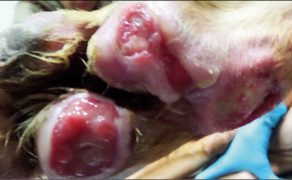
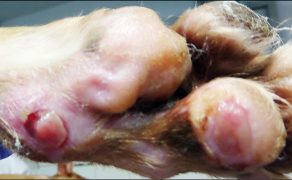
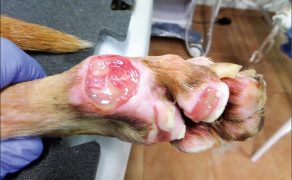
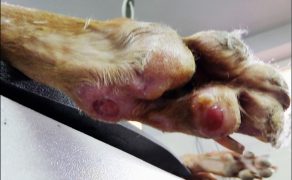
Zastosowanie czynników wzrostu w gojeniu dużych ubytków skórnych i ran przewlekłych u zwierząt towarzyszących
Rodzina PDGF
Płytkopochodny czynnik wzrostu (PDGF) odgrywa istotną rolę w całym procesie gojenia się rany, jest jednym z najsilniejszych stymulatorów gojenia. Jest obecny i pełni istotne funkcje już od pierwszych chwil uszkodzenia i aż do momentu zamknięcia rany (6). Głównym źródłem jest degranulacja płytek krwi, wysokie stężenia są obserwowane w wysięku z rany. PDGF działa chemotaktycznie na neutrofile, monocyty, skórne fibroblasty oraz mezenchymalne komórki macierzyste obecne w szpiku. Istotną rolę odgrywają w fazie zapalnej, stymulują hemopoetyczne komórki macierzyste w kierunku linii mielodialnej.
Badania wykazały, że mogą one dawać początek fibroblastom i keratynocytom (7, 8). Receptory dla PDGF znajdują się również na komórkach śródbłonka – ma to znaczenie w angiogenezie (5). W późniejszych fazach gojenia PDGF wpływa na wytwarzanie składników ECM i proliferację fibroblastów oraz indukuje zmianę fenotypu fibroblastów w miofibroblasty (4). Faza remodelowania PDGF wpływa na rozkład starego kolagenu poprzez aktywację metaloproteinaz macierzy zewnątrzkomórkowej (11). W badaniach doświadczalnych wykazano, iż bardzo wysokie stężenia PDGF aplikowane bezpośrednio na ranę powodują szybsze powstawanie ziarniny oraz zamykanie się rany (9). Obniżone stężenie tego czynnika jest jedną z przyczyn wystąpienia opóźnionego gojenia (10). Wykazano, że PDGF jest wrażliwy na proteolityczne środowisko rany przewlekłej; ulega wówczas degradacji (12).
Rodzina fibroblastycznych czynników wzrostu (FGF)
Zaliczamy tutaj aż 23 czynniki, z czego 3 mają istotne znaczenie w przebiegu gojenia się ran – FGF-2, FGF-7 oraz FGF-10. Niezbędne do aktywacji receptora FGF są proteoglikany i heparyna, które działają na FGF stabilizująco (17). Poziom w FGF-2 (nazywany też zasadowym FGF) zaraz po uszkodzeniu skóry ulega podwyższeniu. Czynnik ten odgrywa ważną rolę w tworzeniu się ziarniny, epitelializacji oraz w przebudowie nowo powstającej tkanki (18).
W badaniach in vitro wykazano, że FGF-2 reguluje syntezę i odkładanie się składników ECM, zwiększa ruchliwość keratynocytów podczas naskórkowania (19), a także promuje migrację fibroblastów i stymuluje je do produkcji kolagenaz (20). Udowodniony jest niższy poziom FGF-2 w ranach przewlekłych (21). Stosowany u pacjentów z odleżynami wykazuje skuteczność w szybszym zamykaniu się rany (22). FGF-2 stymuluje dojrzałe komórki śródbłonka oraz ich prekursory do migracji i podziałów mitotycznych (23). FGF-7, określany inaczej jako czynnik wzrostu keratynocytów (KGF-1), oraz FGF-10 (KGF-2) wytwarzane są natychmiast po uszkodzeniu skóry i stymulują proliferację keratynocytów.
Rodzina naskórkowych czynników wzrostu (EGF)
Do rodziny naskórkowego czynnika wzrostu (EGF) zaliczamy wiele mitogenów. Kluczowymi dla procesu gojenia są: EGF (naskórkowy czynnik wzrostu), TGF-α, HB-EGF (wiążący heparynę EGF-podobny czynnik wzrostu), epiregulina, amfiregulina, heregulina oraz neureguliny -1-6 (NRG-1), NRG-2, NRG-3, NRG-4, NRG-5 i NRG-6, wytwarzane głównie przez makrofagi i neutrofile. Ich zadaniem jest regulacja proliferacji keratynocytów. Ich funkcją jest stymulowanie migracji oraz proliferacji komórek naskórka, wpływają również na aktywność fibroblastów. Badania in vitro dowiodły, że EFG znacznie przyśpiesza naskórkowanie rany (13) oraz zwiększa wytrzymałość rany na rozciąganie (14). Badania in vivo nad TGF-α wskazują na wpływ tego czynnika na wczesną epitelializację rany (15). Ponadto ostatnie badania in vitro wskazują na ich możliwą rolę w angiogenezie (16).
Rodzina transformującego czynnika wzrostu beta, TGF-β (ang. transforming growth factor β)
W gojeniu ubytków skórnych udział biorą przede wszystkim 3 białka TGF-β1-3; są zaangażowane właściwie na każdym etapie gojenia się rany. Izoforma TGF-β3 przeważa w życiu płodowym, dzięki niej skóra płodu goi się bez powstawania blizny. TGF-β1 jest istotny w przebiegu procesów zapalnych, angiogenezie i naskórkowaniu, a także regeneracji tkanki łącznej. TGF-β1 ułatwia rekrutację dodatkowych komórek zapalnych, pośredniczy w zwiększaniu ilości makrofagów, a tym samym w oczyszczeniu tkanki (24). Badania in vitro pokazują, że TGF-β1 pomaga inicjować powstawanie ziarniny poprzez zwiększenie ekspresji genów związanych z tworzeniem ECM, w tym: fibronektyny, receptora fibronektyny, kolagenu oraz inhibitorów proteaz (34).
Jest również zaangażowana w regulację działania czynnika wzrostu śródbłonka naczyniowego VEGF (ang. vascular endothelial growth factor) (25), wpływa na formowanie się macierzy zewnątrzkomórkowej, uczestniczy w produkcji kolagenu typ I i II. Jest także silnym inhibitorem metaloproteinaz MMP-1, MMP-3 oraz MMP-9 i promotorem syntezy tkankowego inhibitora metaloproteinazy TIMP-1, hamującego podział kolagenu (26). Izoforma TGF-β2 bierze udział w rekrutacji komórek zapalnych i fibroblastów, angiogenezie, przyśpiesza epitelializację, uczestniczy w tworzeniu i przebudowie macierzy zewnątrzkomórkowej oraz w produkcji kolagenu (27). Trzecia izoforma, TGF-β3, promuje gojenie ran poprzez rekrutację fibroblastów i ułatwienie migracji keratynocytów. TGF-β3 jest również silnym stymulatorem neowaskularyzacji (29). Jednak w przeciwieństwie do pozostałych dwóch izoform, które pobudzają tworzenie blizn, TGF-β3 hamuje bliznowacenie i promuje lepszą organizację kolagenu (28). W ranach przewlekłych odnotowano zdecydowany spadek stężenia TGF-β, prawdopodobnie ma to związek niedoborem protegolikanów (35).
Galeria
Mogą zainteresować Cię również
Znajdź swoją kategorię
2843 praktycznych artykułów - 324 ekspertów - 23 kategorii tematycznych
Weterynaria w Terenie

Mykotoksyny – ukryty wróg w hodowli bydła mlecznego
Toksyny T-2 i HT-2 Toksyny T-2 i HT-2 należą do grupy trichotecenów i są produkowane głównie przez grzyby z rodzaju Fusarium. Występują w zbożach, szczególnie w owsie, jęczmieniu i kiszonkach traw. Toksyny te, podobnie jak DON, na poziomie molekularnym działają na inhibicję syntezy białek, mogą również powodować uszkodzenia DNA i RNA. Wysokie poziomy trichotecenów mogą […]
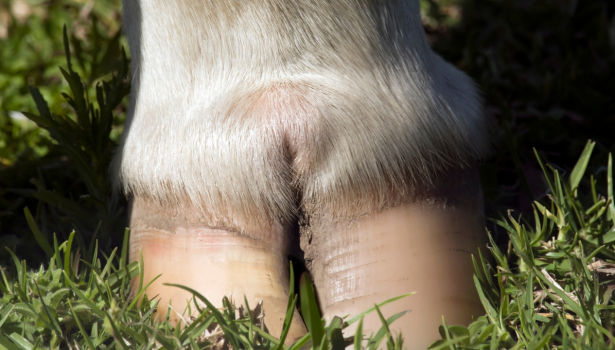
Kulawizna u bydła mlecznego (choroba Mortellaro). Skuteczne zwalczanie zapalenia skóry palca dzięki naturalnemu rozwiązaniu
Biodevas Laboratoires opracowała PIETIX – rozwiązanie w 100% naturalne, mające na celu zwalczenie zapalenia skóry palca u bydła mlecznego.

Czynniki wpływające na kolonizację mikrobiomu i dojrzałość układu pokarmowego prosiąt oraz jego prawidłowe funkcjonowanie
We współczesnym chowie trzody chlewnej wczesne odsadzanie jest skutecznym sposobem na poprawę produktywności loch, ale może również powodować stres odsadzeniowy u prosiąt. Odsadzanie to jeden z najtrudniejszych okresów w życiu prosiąt, który powoduje u nich ogromny stres i towarzyszy mu uszkodzenie morfologii oraz przepuszczalności jelit, a także wpływa na skład mikrobiomu (50). Ponadto po odsadzeniu […]

Opieka stomatologiczna nad starszymi końmi
Pacjenci geriatryczni są grupą wymagającą szczególnej troski w wielu aspektach zdrowotnych. Opieka stomatologiczna w tej grupie jest także niezwykle istotnym elementem mającym wpływ na zdrowie. Stan uzębienia ma ogromny wpływ na dobrostan konia, ponieważ wiele schorzeń stomatologicznych, zwłaszcza u koni geriatrycznych, wiąże się z ogromnym bólem. W praktyce weterynaryjnej za pacjentów starszych uznaje się konie […]

Praktyka w terenie – jak zabezpieczyć się na wypadek stanów zagrożenia życia lub zdrowia zwierzęcia
Odesłanie do innego zakładu Pamiętaj, że chociaż właściciel zgłosi się do ciebie ze zwierzęciem w stanie zagrożenia życia lub zdrowia, może zdarzyć się sytuacja, kiedy będziesz musiał odesłać go do innego zakładu leczniczego. W szczególności gdy twój zakład nie dysponuje właściwym wyposażeniem, aparaturą czy sprzętem w zależności od posiadanej kategorii: gabinetu weterynaryjnego, przychodni weterynaryjnej, lecznicy […]

Wiek ma ogromne znaczenie podczas stawiania diagnozy
Lek. wet. Justyna Domagała tytuł inżyniera zootechniki uzyskała w 2016 r., a tytuł lekarza weterynarii – w 2019 r. na Uniwersytecie Przyrodniczym we Wrocławiu. Po studiach swoją wiedzę poszerzała podczas stażu w Szpitalu dla Koni Equivet, w którym później uzyskała zatrudnienie. W latach 2021-2024 swoją pracę skupiała na internistycznym leczeniu koni oraz pogłębianiu wiedzy na […]
Echa 32. Kongresu Bujatrycznego w Cancun
Profilaktyka Kongres był również okazją do zaprezentowania kilku przełomowych produktów immunologicznych, które mają szansę wprowadzić na nowe tory prewencję znanych od lat jednostek chorobowych, sprawiających wiele kłopotów z punktu widzenia odchowu cieląt czy rozrodu. Mowa tu konkretnie o trzech nowych szczepionkach mających zastosowanie w profilaktyce Mycoplasma bovis, Cryptosporidium parvum czy wirusowej biegunki bydła (BVD). Nie […]