Koronawirusy patogenne dla trzody chlewnej – wirus zakaźnego zapalenia żołądka i jelit
Odporność
Jak wspomniano we wcześniejszej części artykułu, zakażenie PRCV zapewnia częściową odporność przeciwko TGEV, co doprowadziło do zmniejszenia znaczenia klinicznego TGE w wielu krajach. Częściowa odporność jest indukowana przez szybki wzrost miana przeciwciał neutralizujących po narażeniu na TGEV oraz wzrost liczby komórek syntetyzujących immunoglobuliny klasy G (IgG) i A (IgA) w tkance jelit u świń wcześniej zakażonych PRCV (42-44).
Świnie, które przeszły TGE, są odporne przez krótki okres na ponowne zakażenie dzięki lokalnej odporności błon śluzowych i swoistym sekrecyjnym IgA wytwarzanym przez komórki błony śluzowej jelit (42, 44-46). Na czas trwania odporności mają wpływ wiek i status immunologiczny zwierzęcia w momencie pierwotnej infekcji (47). Lochy przekazują nowo narodzonym prosiętom przeciwciała neutralizujące TGEV, zapewniając w ten sposób kluczową w pierwszych dniach życia prosiąt bierną odporność laktogenną, która zabezpiecza przez zakażeniem ogólnoustrojowym (3, 48). Najbardziej efektywną ochronę zapewniają IgA powstające po infekcji drogą pokarmową. Przeciwciała IgA i IgG (szczególnie IgA) wytworzone po reinfekcji loch ciężarnych PRCV zapewniają również ochronę prosiąt przed negatywnymi konsekwencjami TGEV (7).
Diagnostyka
Dodatkowe badania laboratoryjne są niezbędne do potwierdzenia podejrzenia TGE, ponieważ objawy kliniczne i zmiany anatomopatologiczne nie pozwalają na postawienie ostatecznego rozpoznania. W diagnostyce różnicowej należy uwzględnić inne patogeny wykrywane u młodych prosiąt, m.in. PEDV, rotawirusy czy Escherichia coli (7). Materiałem wykorzystywanym w diagnostyce mogą być: zwłoki świeżo padłych prosiąt, wycinki jelit lub zeskrobiny pobrane z błony śluzowej jelita czczego albo krętego, kał lub surowica (33).
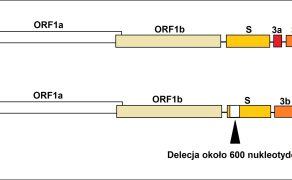
Najczęściej wykorzystywaną metodą diagnostyczną jest wykrywanie materiału genetycznego TGEV za pomocą metody RT-PCR lub RT-PCR w czasie rzeczywistym. W tym celu najlepiej pobrać próbki kału od zwierząt, które uległy zakażeniu 2-7 dni wcześniej. Metoda ta pozwala na odróżnienie zakażenia PRCV od TGE, dzięki obecności delecji w regionie genu S u PRCV. W celu wykrywania przeciwciał przeciwko TGEV metodami serologicznymi (ELISA) bada się surowicę świń, które wykazywały objawy chorobowe TGE przynajmniej tydzień wcześniej. Należy pamiętać, że powstawanie przeciwciał neutralizujących przeciwko TGEV może być także indukowane przez PRCV. Wzrost miana przeciwciał po ostrym okresie choroby przebiegającej ze wzrostem śmiertelności wśród prosiąt i nieżytem przewodu pokarmowego może świadczyć o infekcji TGEV lub PRCV. Przeciwciała neutralizujące przeciwko TGEV mogą być wykrywane nawet przez 18 miesięcy po zakażeniu.
Do testów serologicznych, które pozwalają na różnicowanie między zakażeniem PRCV i TGEV, należy test w formacie blokującym (bELISA), który wykorzystuje fragmenty antygenowe proteiny S nieobecne w przypadku PRCV. We własnym zakresie można przeprowadzić uproszczone badanie diagnostyczne polegające na ocenie stanu kosmków jelitowych pod mikroskopem lub silną lupą. Fragment jelita należy zanurzyć na szkiełku zegarkowym lub szalce Petriego w roztworze płynu fizjologicznego, a następnie ocenić stopień zniszczenia kosmków jelitowych. Przy TGE dochodzi do ich całkowitego zniszczenia. Badania histopatologiczne oraz izolacja wirusa i badania immunohistochemiczne, immunofluorescencja czy mikroskopia elektronowa mogą być również stosowane w diagnostyce TGE, jednak rzadko korzysta się z nich w praktyce (7, 33).
Leczenie
Nie opracowano dotychczas leku przeciwwirusowego przeciwko TGEV i jedynym rozwiązaniem jest leczenie objawowe i zapewnienie zwierzętom najlepszych warunków do wyzdrowienia. Podawanie płynów, elektrolitów i składników odżywczych pozajelitowo u świń jest niepraktyczne w warunkach fermowych, ale alternatywą może być podawanie płynów zawierających zbilansowany zestaw elektrolitów i glukozy doustnie. Konieczne jest zapewnienie warunków środowiskowych pozwalających na szybkie wyzdrowienie prosiąt: dodatkowego źródła ciepła dla osesków (pod którym temperatura wyniesie powyżej 32°C) oraz suchego i czystego kojca. W przypadku koinfekcji bakteryjnych wskazana jest antybiotykoterapia (7). Dopuszcza się także dostawianie prosiąt podatnych lub zainfekowanych TGEV do immunizowanych loch, których siara lub mleko zapewnią prosiętom odporność bierną (49).
Galeria
Mogą zainteresować Cię również
Znajdź swoją kategorię
2640 praktycznych artykułów - 324 ekspertów - 22 kategorii tematycznych
Weterynaria w Terenie

Niezakaźne przyczyny chorób kończyn u świń
Problem kulawizn u loch Kulawizny u loch są, tuż po problemach w rozrodzie, najważniejszą przyczyną brakowań loch z dalszej hodowli. Najwięcej przypadków obserwuje się w okresie od odsadzenia do momentu porodu. Bardzo często schorzenia kończyn są rejestrowane u pierwiastek lub u loch po drugim porodzie, a więc w okresie, kiedy wchodzą one w najbardziej wydajny […]

Posocznica cieląt wywołana przez E. coli. Kolisepticemia
Zapobieganie W przypadku zachorowań na kolisepticemię należy brać pod uwagę przede wszystkim dwa czynniki: niski poziom immunoglobulin w surowicy krwi oraz system odchowu cieląt sprzyjający zakażeniom patogennymi szczepami E. coli (14, 17, 18). Wiele czynników ma wpływ na transfer immunoglobulin siarowych. Jednak najważniejszą rolę odgrywają czas, w jakim zostanie podana siara po urodzeniu, oraz ilość […]

Niezakaźne przyczyny chorób kończyn u świń
Problem kulawizn u loch Kulawizny u loch są, tuż po problemach w rozrodzie, najważniejszą przyczyną brakowań loch z dalszej hodowli. Najwięcej przypadków obserwuje się w okresie od odsadzenia do momentu porodu. Bardzo często schorzenia kończyn są rejestrowane u pierwiastek lub u loch po drugim porodzie, a więc w okresie, kiedy wchodzą one w najbardziej wydajny […]

Kiedy warto zlecić rozmaz krwi u koni?
Po drugie, w rozmazie możliwe jest postawienie podejrzenia aglutynacji erytrocytów, sugerującej immunohemolityczne tło niedokrwistości – IMHA (ryc. 3). Weryfikacja występowania aglutynacji następuje w teście aglutynacji szkiełkowej. Niedokrwistości immunohemolitycznej może także towarzyszyć obecność sferocytów (choć rzadko spotykana u koni). W przypadku hemolizy na tle uszkodzeń oksydacyjnych erytrocytów (np. w przypadku zatruć liśćmi czerwonego klonu lub DMSO) […]
Wskazówki na wypadek widocznego niepowodzenia terapii antybiotykowej. Kryteria skutecznej terapii oraz kluczowe pytania jako 5 kroków drzewa analitycznego
Czynniki powiązane z użyciem antybiotyku w terapii: Czy wybór antybiotyku opierał się na badaniach klinicznych i dodatkowych (diagnoza, antybiogram)? Sprawdź odpowiedź na pytanie 3. Farmakokinetyka/farmakodynamika wybranego antybiotyku? Koncentracja i czas działania antybiotyku w zakażonej tkance a efektywność w stosunku do czynnika bakteryjnego wywołującego chorobę (spektrum działania antybiotyku, wrażliwość z antybiogramu – odpowiedzi na pytanie 3.). […]

Czarno na białym – mastitis okiem praktyka – rozmowa z dr. n. wet. Sebastianem Smulskim
Rozmowa z dr. n. wet. Sebastianem Smulskim, pracownikiem Uniwersytetu Przyrodniczego w Poznaniu, specjalistą w dziedzinie profilaktyki i leczenia mastitis u krów, który w swoich badaniach zgłębia tematykę zapalenia gruczołu mlekowego u bydła, zarówno w aspekcie naukowym, jak i praktycznym. Większość zapaleń gruczołu mlekowego ma etiologię bakteryjną. Dlaczego, pomimo rozwoju mikrobiologii, medycyny weterynaryjnej i prowadzonych badań, […]

XVIII FORUM ZOOTECHNICZNO-WETERYNARYJNE: NOWE HORYZONTY W ROZRODZIE ZWIERZĄT
Na Uniwersytecie Przyrodniczym w Poznaniu w dniach 18-19 kwietnia br. odbyło się XVIII Forum Zootechniczno-Weterynaryjne pod hasłem „Rozród zwierząt w dobie selekcji genomowej”. To wydarzenie zgromadziło liczne grono lekarzy weterynarii oraz hodowców, by omówić najnowsze osiągnięcia w dziedzinie hodowli i rozrodu zwierząt. Organizacja Forum była wspólnym przedsięwzięciem Poznańskiego Koła Polskiego Towarzystwa Zootechnicznego, Wielkopolskiego Oddziału Polskiego […]