Koronawirusy patogenne dla trzody chlewnej – wirus zakaźnego zapalenia żołądka i jelit
Wirusowe zapalenie żołądka i jelit (ang. transmissible gastroenteritis – TGE) zostało opisane po raz pierwszy w 1946 roku w Stanach Zjednoczonych (1). Od tego czasu wirus wywołujący TGE wykrywano praktycznie na całym świecie. Chorobę wywołuje wirus zakaźnego zapalenia żołądka i jelit (ang. transmissible gastroenteritis virus – TGEV) należący do rodziny Coronaviridae, rodzaju Alphacoronavirus. Poza tym w obrębie rodzaju Alphacoronavirus zidentyfikowano jeszcze trzy koronawirusy odpowiadające za infekcje związane z układem pokarmowym u świń: koronawirusa płucnego świń (PRCV), wirusa epidemicznej biegunki świń (PEDV) oraz koronawirusa zespołu ostrej biegunki świń (SADS-CoV) (2). W przebiegu TGE obserwuje się intensywną biegunkę, wymioty i wysoką śmiertelność wśród prosiąt w wieku poniżej dwóch tygodni (3). Zakażenie wspomnianymi wirusami wywołuje u trzody chlewnej chorobę o identycznym obrazie klinicznym, dlatego do wykrywania TGEV ważna jest diagnostyka różnicowa oparta na badaniach laboratoryjnych.
Czynnik etiologiczny TGE
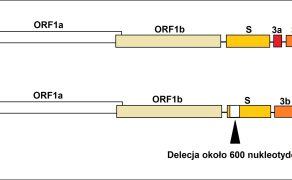
Materiał genetyczny TGEV ma postać RNA o dodatniej polaryzacji, a długość genomu wynosi około 28,5 tysięcy par zasad (4, 5). Genom zawiera tzw. regiony 3` i 5` nieulegające translacji oraz dziewięć ramek odczytu (ang. open reading frame – ORF) pełniących różne funkcje (2). Dwie trzecie genomu TGEV zawiera dwa duże ORF-y, 1a i 1b, kodujące dwie niestrukturalne proteiny, które kierują replikacją genomu i transkrypcją. Pozostała część genomu zawiera ORF-y określające białka strukturalne i niestrukturalne: białko kolca (S), ORF3, białko otoczki (E), glikoproteinę transmembranową (M) i nukleoproteinę (N).
Opisana struktura genomu jest typowa dla wszystkich koronawirusów (2). Białko kolca w dużym stopniu odpowiada za zjadliwość wirusa i odgrywa znaczącą rolę w procesie wnikania wirusa do komórek gospodarza (6). Mutacje w obrębie tego białka mogą wpływać na zmiany w zakresie zjadliwości i tropizmu TGEV (6, 7). Na podstawie sekwencji nukleotydowej ORF3 wśród szczepów TGEV można wyróżnić klaster Miller i klaster Purdue. ORF3 TGEV zawiera sekwencje kodujące niestrukturalne proteiny 3a i 3b. Delecje w obrębie sekwencji kodującej proteinę 3a mogą powodować zmiany w zjadliwości i tropizmie wirusa, a także skutkować całkowitą utratą ORF3a z genomu (8).
Genom TGEV zawiera także ORF7 (6) (ryc. 1).
TGEV jest wrażliwy na wysoką temperaturę, światło słoneczne i promieniowanie ultrafioletowe (7, 9, 10). Pozostaje infekcyjny w płynnych odchodach ponad 8 tygodni w temperaturze 5°C, a w temperaturze 35°C – tylko przez 24 godziny (11). Jego stabilność w niskich temperaturach jest związana z częstszymi wybuchami TGE w okresie zimowym. Wirus jest skutecznie inaktywowany 0,03-proc. formaliną, 1-proc. roztworem fenolu i aldehydu, nadtlenkiem wodoru, środkami dezynfekcyjnymi na bazie jodu, chloroformem czy czwartorzędowymi solami amoniowymi (7).
Występowanie TGEV na świecie
Choroba o przebiegu i cechach charakterystycznych dla TGE została opisana po raz pierwszy w 1935 r., chociaż sam czynnik etiologiczny został zidentyfikowany ponad 10 lat później (1, 12). TGEV prawdopodobnie krążył wcześniej w populacji trzody chlewnej bez znaczącego wpływu na produkcję i zdrowie, stając się ważnym czynnikiem patogennym świń wraz z intensyfikacją produkcji (12). Wirus ten był izolowany na całym świecie w ciągu kolejnych 20 lat od pierwszej identyfikacji. TGE znajduje się także na liście chorób, których wystąpienie należy zgłosić do Światowej Organizacji Zdrowia Zwierząt (WOAH – World Animal Health Organisation).
Według danych z systemu WAHIS (World Animal Health Information System) choroba wystąpiła trzy razy wśród państw członkowskich: w Polinezji Francuskiej i Peru w 2011 r. oraz w Argentynie w 2014 r. (13). Badania dotyczące występowania TGEV są przeprowadzane w Stanach Zjednoczonych i Chinach. W Stanach Zjednoczonych ogólna prewalencja wynosiła 2,3% (667/29 397 próbek kału i tkanek jelit), wahała się od 0,1% do 6,8% w latach 2008-2016, osiągając najniższą wartość w latach 2015-2016 (14). W Chinach materiał genetyczny wirusa wykryto w 0,7% (21/2987) próbek kału pobieranych w latach 2012-2018 (15). Odnotowuje się także występowanie zjadliwych szczepów TGEV w tym kraju. W 2020 r. wyizolowano szczep JS2012 (6).
Zakażenie eksperymentalne tym szczepem skutkowało 100-proc. śmiertelnością nowo narodzonych prosiąt (6). Kolejny zjadliwy szczep TGEV, SC2021, wyizolowano w 2023 r. (16). Sekwencja genomowa wirusa wykazała delecję 81 nukleotydów w ORF3a, co skutkowało brakiem ekspresji niestrukturalnej proteiny 3a oraz prawdopodobnie zwiększeniem zjadliwości i zmianą w powinowactwie wirusa do komórek układu oddechowego. W trakcie badania nie zauważono znaczących objawów z układu oddechowego, jednak szczep SC2021, oprócz zmian charakterystycznych dla TGE, powodował także poważne uszkodzenie tkanki płucnej prosiąt. TGE u prosiąt zakażonych tym szczepem przebiegało z silnie wyrażonymi objawami i wysoką śmiertelnością (16).
Brak jest najnowszych badań epidemiologicznych w aspekcie zakażeń TGEV w wielu krajach, ale mimo to wydaje się, że jest on prawie nieobecny w Europie (17). Zgodnie z obowiązującą Ustawą z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt TGE podlega w Polsce obowiązkowi rejestracji. Aktualnie brak oficjalnych zgłoszeń dotyczących występowania TGEV w Polsce.
W ostatnich latach odnotowuje się koinfekcje TGEV z innymi, m.in. PEDV oraz PRCV (18-20). Wymienione wirusy należą do alfa-koronawirusów patogennych dla świń, a koinfekcje wśród tej grupy są częste. Notowane są rekombinacje pomiędzy TGEV a PEDV, co może skutkować powstawaniem szczepów TGEV o nowych właściwościach, w tym wirusów o zwiększonej zjadliwości (21).
Galeria
Mogą zainteresować Cię również
Znajdź swoją kategorię
2640 praktycznych artykułów - 324 ekspertów - 22 kategorii tematycznych
Weterynaria w Terenie

Niezakaźne przyczyny chorób kończyn u świń
Problem kulawizn u loch Kulawizny u loch są, tuż po problemach w rozrodzie, najważniejszą przyczyną brakowań loch z dalszej hodowli. Najwięcej przypadków obserwuje się w okresie od odsadzenia do momentu porodu. Bardzo często schorzenia kończyn są rejestrowane u pierwiastek lub u loch po drugim porodzie, a więc w okresie, kiedy wchodzą one w najbardziej wydajny […]

Posocznica cieląt wywołana przez E. coli. Kolisepticemia
Do organizmu nowo narodzonych cieląt patogenne szczepy E. coli mogą wnikać różnymi drogami. Najważniejszą rolę spośród nich odgrywa nabłonek jelit. Wnikanie odbywa się na drodze pinocytozy, w czasie pełnej przepuszczalności nabłonka jelit (3). Innymi drogami wniknięcia drobnoustrojów mogą być błona śluzowa nosa, jamy ustnej i gardła oraz pępek (6, 7). U zakażonych cieląt przebieg choroby […]

Niezakaźne przyczyny chorób kończyn u świń
Problem kulawizn u loch Kulawizny u loch są, tuż po problemach w rozrodzie, najważniejszą przyczyną brakowań loch z dalszej hodowli. Najwięcej przypadków obserwuje się w okresie od odsadzenia do momentu porodu. Bardzo często schorzenia kończyn są rejestrowane u pierwiastek lub u loch po drugim porodzie, a więc w okresie, kiedy wchodzą one w najbardziej wydajny […]

Kiedy warto zlecić rozmaz krwi u koni?
Co może wnieść mikroskopowa ocena komórek krwi w diagnostyce chorób koni? W jakich przypadkach rozmaz krwi u tego gatunku może być przydatny, a w jakich mniej? Co zrobić, żeby zmaksymalizować wartość diagnostyczną badania i jak interpretować jego wynik? Artykuł ma na celu odpowiedź na te – i kilka innych – często zadawanych pytań. Jest on […]
Wskazówki na wypadek widocznego niepowodzenia terapii antybiotykowej. Kryteria skutecznej terapii oraz kluczowe pytania jako 5 kroków drzewa analitycznego
Czynniki powiązane z użyciem antybiotyku w terapii: Czy wybór antybiotyku opierał się na badaniach klinicznych i dodatkowych (diagnoza, antybiogram)? Sprawdź odpowiedź na pytanie 3. Farmakokinetyka/farmakodynamika wybranego antybiotyku? Koncentracja i czas działania antybiotyku w zakażonej tkance a efektywność w stosunku do czynnika bakteryjnego wywołującego chorobę (spektrum działania antybiotyku, wrażliwość z antybiogramu – odpowiedzi na pytanie 3.). […]

Czarno na białym – mastitis okiem praktyka – rozmowa z dr. n. wet. Sebastianem Smulskim
Rozmowa z dr. n. wet. Sebastianem Smulskim, pracownikiem Uniwersytetu Przyrodniczego w Poznaniu, specjalistą w dziedzinie profilaktyki i leczenia mastitis u krów, który w swoich badaniach zgłębia tematykę zapalenia gruczołu mlekowego u bydła, zarówno w aspekcie naukowym, jak i praktycznym. Większość zapaleń gruczołu mlekowego ma etiologię bakteryjną. Dlaczego, pomimo rozwoju mikrobiologii, medycyny weterynaryjnej i prowadzonych badań, […]

XVIII FORUM ZOOTECHNICZNO-WETERYNARYJNE: NOWE HORYZONTY W ROZRODZIE ZWIERZĄT
Na Uniwersytecie Przyrodniczym w Poznaniu w dniach 18-19 kwietnia br. odbyło się XVIII Forum Zootechniczno-Weterynaryjne pod hasłem „Rozród zwierząt w dobie selekcji genomowej”. To wydarzenie zgromadziło liczne grono lekarzy weterynarii oraz hodowców, by omówić najnowsze osiągnięcia w dziedzinie hodowli i rozrodu zwierząt. Organizacja Forum była wspólnym przedsięwzięciem Poznańskiego Koła Polskiego Towarzystwa Zootechnicznego, Wielkopolskiego Oddziału Polskiego […]