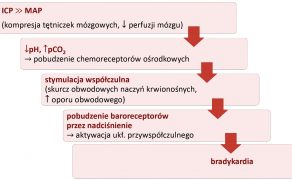
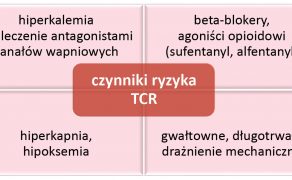
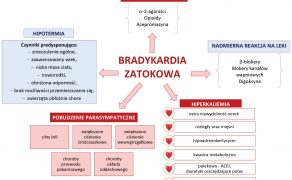
Bradykardia zatokowa u psów
Leczenie bradykardii
Z uwagi na specyfikę etiologiczną i podstawy patofizjologiczne dwóch głównych rodzajów bradyarytmii spotykanych w praktyce klinicznej (czyli bradykardii odruchowej i przewlekłej, chorobowej) ich leczenie istotnie się różni.
Wszystkie bradykardie zatokowe występujące nagle to często stany odruchowe czy też wywołane jatrogennie, związane ze znieczuleniem ogólnym, manipulacją chirurgiczną czy zastosowanymi lekami. W większości przypadków wystarczą uważny monitoring pacjenta i zaniechanie dalszego podawania leku odpowiedzialnego za wywołanie bradykardii, tudzież odstąpienie od manipulacji na obszarze zaopatrywanym przez nerwy biorące udział w powstawaniu wyżej opisanych odruchów. Z uwagi na uczestnictwo układu parasympatycznego w powstawaniu tych odruchów w leczeniu można wykorzystać atropinę (10), a w przypadkach opornych niezbędne może okazać się zastosowanie agonisty receptora β1-adrenergicznych – dopaminy (3).
Wśród wskazań do implantacji sztucznego stymulatora serca Santilli i in. (38) wymienili: zaawansowany blok przedsionkowo-komorowy drugiego i trzeciego stopnia (AVB II i III, ang. 2nd and 3rd degree atrioventricular block), zespół chorej zatoki (SSS, ang. sick sinus syndrome), zahamowanie akcji przedsionków (AS, ang. atrial standstill), jak również omdlenia wazowagalne (18, 38). Oczywiście, jak każda procedura medyczna, implantacja stymulatora serca jest związana z ryzykiem wystąpienia powikłań. Do najczęstszych komplikacji pozabiegowych zalicza się: infekcje, nagromadzenie się surowiczego płynu w obszarze tkanki podskórnej w miejscu implantacji stymulatora czy przemieszczenie elektrody – występują one jednak z niewysoką częstością, nieprzekraczającą 10,8% pacjentów (40). Wprowadzenie list kontrolnych jako elementu dobrej praktyki chirurgicznej istotnie zmniejsza ryzyko wystąpienia poważnych komplikacji podczas tego zabiegu (50).
Implantacja sztucznego stymulatora serca to jedyne skuteczne postępowanie w celu poprawy jakości i wydłużenia życia psów z objawową bradyarytmią. Jak dowodzą wyniki badań Johnson i in. (20), metoda ta cechuje się blisko 90-proc. skutecznością w eliminowaniu objawów u psów z blokiem przedsionkowo-komorowym III stopnia lub zespołem chorej zatoki. W przypadkach omdleń wazowagalnych u 6/8 psów doszło do istotnego spadku częstotliwości omdleń, a pozostałe dwa psy po implantacji rozrusznika nie wykazywały ich wcale (20).
Obecnie są prowadzone intensywne badania naukowe mające na celu opracowanie biologicznych metod stymulacji z zastosowaniem komórek progenitorowych kardiomiocytów hCPCs (ang. human cardiomyocyte progenitor cells) (47) lub ludzkich mezenchymalnych komórek macierzystych (hMSC) (48). Co ciekawe, w jednym z badań wykorzystano model psi i modyfikowane za pomocą mysiego genu dla kanału potasowego – HCN4 (ang. hyperpolarization-activated cyclic-nucleotide gated potassium channel 4) psie macierzyste komórki mezenchymalne (cMSC) wszczepiono podnasierdziowo (w lewą komorę serca) psom z eksperymentalnie indukowanym całkowitym blokiem przedsionkowo-komorowym. Opisana metoda pozwoliła uzyskać skuteczną stymulację przez okres minimum 6 tygodni z dostosowaniem częstości rytmu serca do aktywności fizycznej (23).
Dalsze badania są niezbędne, by uzyskać dłuższy czas działania tych biologicznych rozruszników oraz opracować najskuteczniejszą metodę transferu genów kodujących kanały jonowe do komórek docelowych, np. przy użyciu lentiwirusów (22). Odpowiednia funkcja błonowych kanałów jonowych jest niezbędna do utrzymania potencjałów elektrycznych na właściwym poziomie, a co za tym idzie – poprawnego działania tych „biologicznych” rozruszników. W osiągnięciu tego celu komórki hCPCs wykazywały się nieco dłuższą aktywnością (do 12 tyg.) niż cMSC. Co więcej, w odróżnieniu od komórek mezenchymalnych nie wykazywały one tendencji do migracji z miejsca implantacji (47). Najnowsze doniesienia dowodzą możliwości potencjalizacji efektu za pomocą podwójnej modyfikacji genomu komórek, to znaczy przy użyciu genów dla kanałów jonowych z rodziny HCN jak również kanału sodowego pozyskanego z komórek mięśni szkieletowych, czyli SkM1 (ang. skeletal muscle sodium channel) (48).
Uwaga!
W przypadkach przewlekłych, objawowych (!) bradyarytmii jedyną możliwością skutecznej terapii jest implantacja sztucznego stymulatora serca (rozrusznika). Nawet jeśli chwilowa reakcja na podanie np. atropiny doprowadzi do wzrostu częstości rytmu zatokowego, nie jest to możliwe w dłuższej perspektywie przy użyciu jedynie leczenia farmakologicznego (np. teofiliny). Dodatkowo, opisany ostatnio przypadek kliniczny 4-letniego pacjenta z chorobą Addisona dowodzi, że nie wszystkie bradyarytmie na tle endokrynopatii są zależne od nerwu błędnego i pacjenci wcale nie muszą zareagować na podanie antagonisty parasympatycznego (25).
Podsumowanie
Temat zwolnionej pracy mięśnia sercowego jest znacznie ciekawszy i obszerniejszy, niż mogłoby się wydawać. Zarówno wśród zjawisk fizjologicznych (nierzadko na granicy patologii), jak i w metodach terapii wciąż pozostaje wiele niewiadomych, które czekają na odkrycie i wyjaśnienie.
Galeria
Mogą zainteresować Cię również
Znajdź swoją kategorię
2618 praktycznych artykułów - 324 ekspertów - 22 kategorii tematycznych
Weterynaria w Terenie

Przypadek zapalenia mózgu i mięśnia sercowego u prosiąt ssących
Testy PCR wykonano na próbkach pulowanych (pule trzech próbek, według wieku prosiąt). Próbki różnych tkanek (tab. 3) utrwalono w zbuforowanej 10-proc. formalinie i zatopiono w parafinie. Skrawki o grubości 5 µm barwiono hematoksyliną i eozyną. Preparaty z serca wykorzystano również do badania immunohistochemicznego z wykorzystaniem własnych przeciwciał monoklonalnych (3E5). Za dodatnie uznawano próbki, w których […]

Podkliniczny niedobór wapnia i jego wpływ na wyniki rutynowych badań laboratoryjnych w różnych okresach laktacji u krów mlecznych
Diagnostyka laboratoryjna Badania bakteriologiczne Ze względu na znaczenie epizootyczne choroby każde podejrzenie pleuropneumonii winno być poparte badaniem bakteriologicznym. Istotnym momentem w badaniu bakteriologicznym jest stosowanie podłoży selektywnych z dodatkiem DPN lub NAD oraz dysponowanie właściwym materiałem biologicznym do badań. Materiał ten musi być pobrany i przekazany do laboratorium nie później niż 24 godziny po padnięciu […]

Przypadek zapalenia mózgu i mięśnia sercowego u prosiąt ssących
Testy PCR wykonano na próbkach pulowanych (pule trzech próbek, według wieku prosiąt). Próbki różnych tkanek (tab. 3) utrwalono w zbuforowanej 10-proc. formalinie i zatopiono w parafinie. Skrawki o grubości 5 µm barwiono hematoksyliną i eozyną. Preparaty z serca wykorzystano również do badania immunohistochemicznego z wykorzystaniem własnych przeciwciał monoklonalnych (3E5). Za dodatnie uznawano próbki, w których […]

Choroby koni. Weterynaria praktyczna. Profilaktyka, rutynowe szczepienia
Publikacja stanowi fragment książki Choroby koni. Weterynaria praktyczna Wirus grypy jest wysoce zaraźliwy i szybko się rozprzestrzenia, a sama choroba niesie ze sobą bardzo poważne skutki i na długi czas wyklucza konia z udziału w zawodach czy wyścigach. Z tego względu wprowadzono wymóg obowiązkowych szczepień przeciwko grypie dla wszystkich koni wyścigowych oraz koni sportowych. Opory […]
Wskazówki na wypadek widocznego niepowodzenia terapii antybiotykowej. Kryteria skutecznej terapii oraz kluczowe pytania jako 5 kroków drzewa analitycznego
Czynniki powiązane z użyciem antybiotyku w terapii: Czy wybór antybiotyku opierał się na badaniach klinicznych i dodatkowych (diagnoza, antybiogram)? Sprawdź odpowiedź na pytanie 3. Farmakokinetyka/farmakodynamika wybranego antybiotyku? Koncentracja i czas działania antybiotyku w zakażonej tkance a efektywność w stosunku do czynnika bakteryjnego wywołującego chorobę (spektrum działania antybiotyku, wrażliwość z antybiogramu – odpowiedzi na pytanie 3.). […]

Czarno na białym – mastitis okiem praktyka – rozmowa z dr. n. wet. Sebastianem Smulskim
Rozmowa z dr. n. wet. Sebastianem Smulskim, pracownikiem Uniwersytetu Przyrodniczego w Poznaniu, specjalistą w dziedzinie profilaktyki i leczenia mastitis u krów, który w swoich badaniach zgłębia tematykę zapalenia gruczołu mlekowego u bydła, zarówno w aspekcie naukowym, jak i praktycznym. Większość zapaleń gruczołu mlekowego ma etiologię bakteryjną. Dlaczego, pomimo rozwoju mikrobiologii, medycyny weterynaryjnej i prowadzonych badań, […]

XVIII FORUM ZOOTECHNICZNO-WETERYNARYJNE: NOWE HORYZONTY W ROZRODZIE ZWIERZĄT
Na Uniwersytecie Przyrodniczym w Poznaniu w dniach 18-19 kwietnia br. odbyło się XVIII Forum Zootechniczno-Weterynaryjne pod hasłem „Rozród zwierząt w dobie selekcji genomowej”. To wydarzenie zgromadziło liczne grono lekarzy weterynarii oraz hodowców, by omówić najnowsze osiągnięcia w dziedzinie hodowli i rozrodu zwierząt. Organizacja Forum była wspólnym przedsięwzięciem Poznańskiego Koła Polskiego Towarzystwa Zootechnicznego, Wielkopolskiego Oddziału Polskiego […]