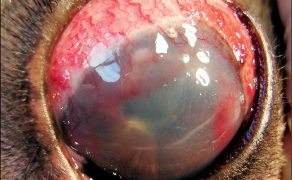
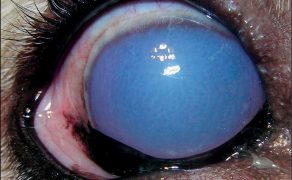
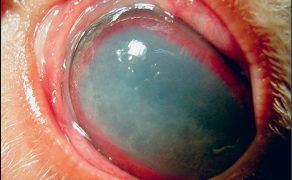
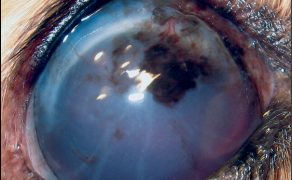
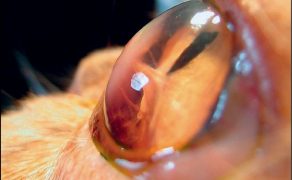
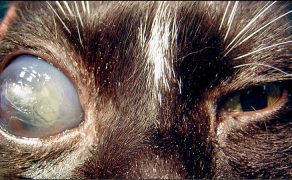
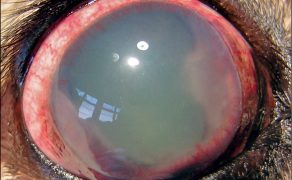
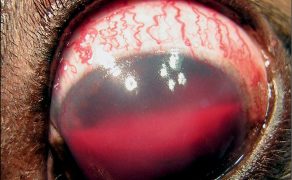
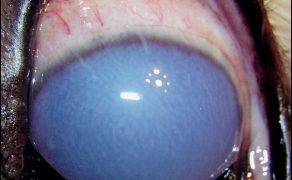
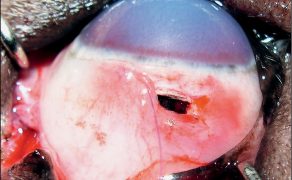
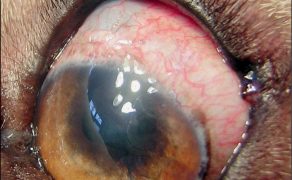
Jaskra – fakty, mity i obecny stan wiedzy
Jaskra jest zespołem chorób oczu przebiegającym z uszkodzeniem komórek zwojowych siatkówki, zanikiem głowy nerwu wzrokowego, postępującym ubytkiem pola widzenia, nieuchronnie prowadzącym do ślepoty oraz nierzadko ze znaczną bolesnością. Dlatego podjęty temat wydaje się bardzo interesujący i niezwykle istotny zarówno z naukowego i klinicznego, jak również utylitarnego i deontologicznego punktu widzenia. Do jednej z najczęściej spotykanych przyczyn i zarazem objawów jaskry zaliczyć należy podwyższone ciśnienie wewnątrzgałkowe (IOP), lecz nie jest to bezwzględną regułą. Diagnostyka jaskry oparta wyłącznie na pomiarze ciśnienia wewnątrzgałkowego była praktyką kliniczną stosowaną do końca lat 50. Jedynym objawem łączonym z jaskrą był ból oka powodowany podwyższonym ciśnieniem. Z czasem wyodrębniono zespoły czynników ryzyka zwiększających prawdopodobieństwo wystąpienia jaskry. Podzielono je na dwie kategorie, z których pierwsza obejmowała naczyniowe czynniki ryzyka: niskie ciśnienie krwi, objawy naczynioskurczowe, cukrzyca, miażdżyca naczyń oraz migreny, a druga obejmowała mechaniczne czynniki ryzyka w postaci: mikroftalmii, krótkowzroczności, IOP zależnego bloku przepływu aksoplazmy na poziomie lamina cribrosa sclerae.
Jeżeli istnieją formy kliniczne jaskry normo- lub hipotensyjnej, a przypadki takie są opisywane u psów, powstaje pytanie o mechanizm tych procesów. Dlatego powszechnie stosowana definicja wymagałaby, najdelikatniej mówiąc, gruntownej modyfikacji. Jak bowiem w myśl powszechnie panującej teorii wyjaśnić przyczynę ubytków widzenia w oku przeciwnym do oka jaskrowego z podwyższonym IOP?
Obecnie rozpoznano kilka alternatywnych mechanizmów prowadzących do uszkodzenia komórek zwojowych siatkówki i w konsekwencji do powstania zespołu jaskry. Wśród nich wymienić należy bloki przepływu aksoplazmy na poziomie lamina cribrosa sclerae, ischemię głowy nerwu wzrokowego zmniejszającą okoliczną perfuzję tkanek (2, 4, 5) oraz wyjątkową wrażliwość komórek zwojowych siatkówki (RGC) o dużej średnicy aksonów na neurotoksyczny wpływ szklistkowego kwasu glutaminowego (1, 5, 13). Przy wysokim niedokrwieniu komórek nerwowych siatkówki wydziela się szklistkowy kwas glutaminowy, bezpośrednio powodujący śmierć neuronów. Teoretycznie leczenie obejmujące zahamowanie wydzielania kwasu glutaminowego pozwoliłoby ochronić komórki nerwowe przed obumieraniem i następową jaskrą. Wrażliwość na kolaps aksonów komórek zwojowych siatkówki jest odwrotnie proporcjonalna do sześcianu ich średnicy. Zatem nawet przy nieznacznych skokach IOP może dochodzić do istotnych zaburzeń w przepływie aksoplazmy, kolapsu aksonów i ich atrofii (2, 4, 5). Bez odpowiedzi zostaje jednak pytanie, dlaczego w pierwszym rzędzie umierają komórki małych włókien?
Badania z University College London wykryły, że w przypadku jaskry komórki zwojowe siatkówki oka produkują za dużo białka α-amyloidowego, przez co powstające złogi, tak samo jak w przypadku choroby Alzheimera, przyczyniają się do rozwoju choroby. W świecie nauki panuje obecnie przeświadczenie, że wykrycie skutecznego leczenia przeciw jaskrze może dać cenne wskazówki względem leczenia choroby Alzheimera. Wyłaniają się tu zatem dwie niezwiązane z IOP teorie dotyczące patogenezy jaskry: naczyniowa i neurotoksyczna, które per se czynią z podwyższonego IOP objaw, a nie przyczynę ślepoty. Teorie te mogą również dać odpowiedź na postawione wcześniej pytania. Co więcej, mogą również wytyczać nowe szlaki terapii przeciw zespołowi jaskry. Leczenie oparte na teorii naczyniowej i neurotoksycznej oscylować będzie wokół stosowania neuroprotektorów i blokerów kanałów wapniowych, podczas gdy klasyczna teoria mechaniczna angażować będzie leczenie inhibujące anhydrazę węglanową, β-blokery, analogi PGF2α, sympatyko/parasympatykomimetyki, hyperosmotyki oraz techniki leczenia chirurgicznego. W niniejszym artykule przedstawiono szereg metod operacyjnego leczenia jaskry z jednoczesnym wskazaniem celowości wyboru określonej procedury, względem poszczególnych przyczyn jaskry u psów.
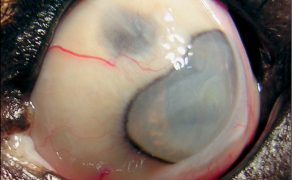
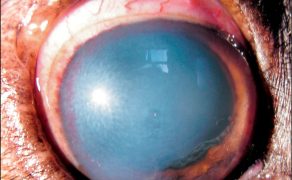
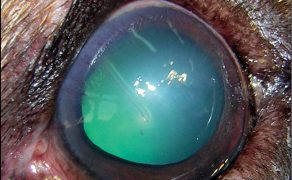
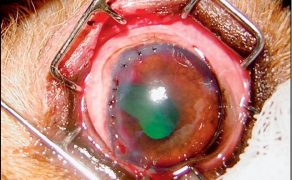
Galeria
Mogą zainteresować Cię również
POSTĘPOWANIA
w weterynarii